Транспозиция магистральных сосудов и дмжп послеоперационный период. Операция артериального переключения. Прогнозы и летальность после операции, длительность и качество жизни
Транспозиция магистральных сосудов (ТМС) – это врожденный сердечный порок, при котором формируется аномалия отхождения центральных сосудов (аорты и легочной артерии) от сердца. В норме аорта несет кровь от левого желудочка, а легочный ствол отходит от правого желудочка. При транспозиции расположение центральных сосудов меняется таким образом, что аорта сообщается с правым желудочком, а ствол легочной артерии – с левым.
Это заболевание встречается, по разным данным, в 7-15 % — 12-20 % среди . Такой порок несовместим с жизнью, то есть при его обнаружении у новорожденного необходимо ургентное оперативное вмешательство. Корригированная транспозиция магистральных сосудов не так сильно сказывается на здоровье детей.
Этиология заболевания
 Факторы, приводящие к формированию порока
Факторы, приводящие к формированию порока
Порок формируется в процессе эмбриогенеза, причины его формирования определить достаточно сложно. Этиологическими факторами могут послужить:
- Заболевания матери во время беременности. К ним относятся ОРВИ, интоксикация любой этиологии, краснуха, корь, сахарный диабет. Неправильное отхождение крупных сосудов может происходить из-за мутагенного воздействия факторов окружающей среды на организм беременной женщины. В частности, речь идет о курении, злоупотреблении спиртными напитками, приеме запрещенных лекарств, недостатке питательных веществ и витаминов.
- Наследственная предрасположенность.
- Хромосомные аномалии. Данный порок, например, встречается у детей с синдромом Дауна.
Если во время ранней перинатальной диагностики выявляются множественные пороки развития плода или имеет место сочетание несовместимых с жизнью изменений, врачи могут предлагать прерывание беременности.
В зависимости от анатомических особенностей развития порока различают две формы заболевания:
- полную транспозицию магистральных сосудов;
- корригированную транспозицию магистральных артерий.
Полная транспозиция магистральных сосудов у детей характеризуется отсутствием сообщения между кругами кровообращения. По аорте, выходящей из правого желудочка, течет не насыщенная кислородом венозная кровь. Она распространяется по всем органам и тканям организма, затем по венам возвращается вновь в правые отделы сердца.
 Виды пороков
Виды пороков
В малом круге кровообращения кровь циркулирует между левыми отделами сердца (предсердием и желудочком) и легкими. То есть кровь насыщается кислородом, но она не может попасть ко всем органам и тканям организма, а циркулирует только по малому кругу кровообращения.
У плода в процессе внутриутробного развития дыхание через легкие не осуществляется, поэтому легочный круг не функционирует. При этом кровь циркулирует через открытое овальное окно, которое в норме есть у каждого плода. После рождения малый круг кровообращения начинает функционировать, и насыщение кислородом должно осуществляться с помощью дыхания через легкие. При полной транспозиции и отсутствии коммуникаций в виде дополнительных пороков ребенок нежизнеспособен и погибает практически сразу после рождения.
Корригированная транспозиция магистральных сосудов – более благоприятная ситуация в плане прогноза и жизнеспособности ребенка на момент рождения. В этом случае с помощью сопутствующего наличия дополнительных пороков сердца (например, или межпредсердной перегородки) осуществляется сообщение между большим и малым кругами кровообращения. Эти коммуникации хоть и не полностью, но в какой-то мере компенсируют состояние пациента.
В 80 % случаев существуют дополнительные коммуникации, с помощью которых организм хотя бы частично компенсирует гемодинамические нарушения. Полная транспозиция с отсутствием сообщения между кругами кровообращения встречается достаточно редко, однако она очень опасна для жизни ребенка.
Клинические проявления и диагностика
Клинику заболевания, в первую очередь, определяют гемодинамические нарушения. Транспозиция магистральных сосудов у новорожденных характеризуется следующими симптомами:
- Вследствие циркуляции по всему организму венозной крови, обедненной кислородом, все тело ребенка имеет синюшный оттенок ().
- Постепенно из-за компенсаторного увеличения объема циркулирующей крови происходит перегрузка сердца. Оно увеличивается в размерах, развивается сердечная недостаточность, которую сопровождают такие симптомы, как , частый пульс, отеки. Происходит увеличение печени.
- Обычно ребенок отстает в физическом развитии, характерна гипотрофия.
- Может формироваться «сердечный горб».
- Изменяется вид фаланг пальцев, они становятся похожими на «барабанные палочки», что характерно при кислородном голодании.
 Транспозиция магистральных артерий
Транспозиция магистральных артерий
Часто при наличии данного порока уже при рождении врач может заподозрить его наличие. На такую мысль, прежде всего, наводит наличие выраженного цианоза кожных покровов у ребенка. Если имеет место корригированная транспозиция магистральных артерий, синюшности при рождении может и не быть. Она может проявиться позже, когда дополнительные пути сообщения кругов кровообращения уже не справляются с обеспечением оксигенированной кровью организма по мере его роста.
Кроме данных физикального обследования, которых обычно не хватает для постановки правильного диагноза, используют также следующие инструментальные методы:
- Эхокардиографию или ультразвуковое исследование (УЗИ) сердца – наиболее доступный и достаточно информативный метод диагностики, который позволяет определить место отхождения аорты и легочной артерии, обнаружить дополнительные пути коммуникации и сопутствующие пороки сердца.
- Рентгенографию грудной клетки — дополнительный метод исследования. Позволяет отметить кардиомегалию (увеличенные размеры сердца), определить положение легочной артерии, обеднение или сгущение легочного рисунка. На снимке можно увидеть, что изменен сосудистый пучок. Он становится широким в боковой проекции и суженным в передне-задней.
- Электрокардиограмма (ЭКГ) не позволяет установить точный диагноз, однако помогает выявить сопутствующие нарушения работы сердца, перегрузки правых отделов, наличие нарушений ритма.
- Анализ парциального напряжения газов и пульсоксиметрия помогают определить степень обогащения крови кислородом.
- Катетеризацию сердца (зондирование полостей) – малоинвазивную процедуру, суть которой заключается в ведении катетера в сердце через бедренную артерию. Таким образом, можно получить информацию о парциальном давлении кислорода в правых и левых отделах сердца, определить давление в сердечных камерах. Будет отмечаться перенасыщение в правых отделах и недостаточная насыщенность кислородом в левых.
- Рентгеновские методы исследования с контрастированием включают коронароангиографию, аортографию, вентрикулографию. С помощью введения контрастного вещества есть возможность визуализации патологического поступления крови из правого желудочка в аорту, а из левого – в легочную артерию. Можно определить наличие сообщений и дополнительных пороков.
Возможности лечения
При транспозиции магистральных сосудов необходимо как можно раньше пройти весь диагностический процесс. Лечение необходимо начинать сразу же после постановки диагноза. Консервативные методы при данном пороке сердца неэффективны, поэтому в таких случаях всегда проводится операция.
 Транспозиция главных артерий
Транспозиция главных артерий
При полной форме транспозиции сосудов проводится экстренное хирургическое лечение, так как существует угроза жизни пациента. Корригированная транспозиция магистральных сосудов также требует хирургического лечения. Однако ситуация не такая ургентная, как при полном варианте из-за частичной компенсации.
Варианты оперативного лечения ТМС:
- Артериальное переключение – вмешательство, при котором кардиохирург осуществляет перемещение крупных сосудов на свои места, то есть соединяет аорту с левым желудочком, а легочную артерию – с правым. Кроме того, проводится коррекция дефектов между камерами сердца при их наличии.
- Операция на предсердиях заключается в осуществлении сообщения между предсердиями. В этом случае венозная кровь может поступать в левые отделы сердца и легочную артерию для обогащения кислородом. При этом сохраняется позиция магистральных артерий, и правый желудочек вынужден прокачивать через себя насыщенную кислородом кровь и доставлять ее по всему организму. Другими словами, он берет на себя функцию левого желудочка. Это может привести к гипертрофии и дилатации правого желудочка, а также спровоцировать различные нарушения сердечного ритма.
- Паллиативная операция проводится в первые дни после появления ребенка на свет при угрозе его жизни. Заключается она в атриальной септостомии – увеличении размеров отверстия в перегородке между предсердиями. Для этого эндоваскулярно вводится корригирующий баллон или проводится резекция межпредсердной перегородки. Цель – осуществление сообщения между предсердиями и, как следствие, сообщения между малым и большим кругами кровообращения. Данная операция выполняется с целью коррекции гемодинамических нарушений для улучшения состояния ребенка и подготовки к проведению основной операции (1 или 2 вариант).
После операции необходимо дальнейшее пожизненное наблюдение кардиолога или кардиохирурга, соблюдение щадящего режима. Ребенок должен избегать тяжелых физических нагрузок, соблюдать режим труда и отдыха, следить за правильным питанием и полноценным сном, проходить периодическое медицинское обследование. Необходимо проведение профилактики .
Прогноз после оперативной коррекции достаточно неплохой – 85-90 % пациентов демонстрируют положительные отдаленные результаты, при сложных пороках сердца – в 65-70 % случаев. При полной транспозиции и отсутствии своевременного лечения прогноз неутешительный – 50 % детей не выживает в течение первого месяца и более 2/3 детей – в течение 1 года жизни. При корригированной транспозиции магистральных артерий выживаемость и прогноз несколько лучше. Однако при отсутствии лечения с возрастом состояние ухудшается. Как последствие нарушений гемодинамики нарастает сердечная недостаточность и другие серьезные осложнения.
Транспозиция магистральных сосудов – очень тяжелая врожденная аномалия, достаточно часто встречающаяся и имеющая серьезные последствия при отсутствии своевременной хирургической коррекции. Большое значение имеет ранняя диагностика. Хорошо, если порок выявлен у плода еще до родов. Зачастую наличие подобного порока не повод, чтобы женщине предложили сделать аборт. Ранняя диагностика дает возможность соответствующего ведения беременности и подготовки к родам. Даже если порок выявлен после родов, своевременная диагностика и лечение помогут сохранить ребенку жизнь.
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК - 2015
Дефект межжелудочковой перегородки (Q21.0), Дефект предсердной перегородки (Q21.1), Дискордантное желудочково-артериальное соединение (Q20.3), Дискордантное предсердно-желудочковое соединение (Q20.5), Другие врожденные аномалии крупных артерий (Q25.8), Открытый артериальный проток (Q25.0)
Кардиохирургия детская, Педиатрия
Общая информация
Краткое описание
Рекомендовано
Экспертным советом
РГП на ПХВ «Республиканский центр
развития здравоохранения»
Министерства здравоохранения
и социального развития
Республики Казахстан
от «30» сентября 2015 года
Протокол № 10
Хирургическое лечение транспозиции магистральных сосудов у детей.
Транспозиция магистральных сосудов - врожденная сердечная аномалия при которой аорта отходит полностью или в значительной степени от правого желудочка, а легочный ствол отходит полностью или в значительной степени от левого желудочка.
Код протокола:
Код(ы) МКБ:
Q20.3 - Транспозиция магистральных сосудов
Q 20.3 - Дискордантное предсердно желудочковой соединение.
Q20.5 - Дискордантное желудочково-предсердное соединение.
Q25.8 - Другие врожденные аномалии крупных артерий
Q21.0 - Дефект межжелудочковой перегородки
Q21.1 - Дефект межпредсердной перегородки
Q25.0 - Открытый артериальный проток
Сокращения, используемые в протоколе:
|
АВ
--
атриовентрикулярный
АоК -- аортальный клапан ВИЧ -- вирус иммунодефицита человека ВПС -- врожденные пороки сердца ДМЖП -- дефект межжелудочковой перегородки ДОС от ПЖ -- двойное отхождение сосудов от правого желудочка ИК -- искусственное кровообращение ИФА -- Иммуноферментный анализ КоА -- коарктация аорты КТ -- компьютерная томография МРТ -- магнитно-резонансная томография ЛА -- легочная артерия ЛГ -- легочная гипертензия ОАП -- открытый артериальный проток ОВТЛЖ - обструкция выводного отдела из левого желудочка ООО -- открытое овальное окно ТМС -- транспозиция магистральных сосудов ЭКГ -- электрокардиограмма ЭхоКГ -- эхокардиография D-ТМС -- простая транспозиция магистральных сосудов L-TMA -- корригированная транспозиция магистральных сосудов PVR -- pulmonary vascular resistance SVR -- systemic vascular resistance АлТ -- аланинаминотрансфераза АсТ -- аспартатаминотрансфераза Q p /Q s - отношение легочного кровотока к системному |
Дата разработки протокола: 2015 год.
Пользователи протокола : детские кардиохирурги, детские кардиологи, неонатологи, педиатры.
Примечание: в данном протоколе используются следующие классы рекомендаций и уровни доказательств:
Классы рекомендаций:
Класс I - польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс II - противоречивые данные и/или расхождение мнений по поводу пользы/эффективности лечения
Класс IIа - имеющиеся данные свидетельствуют о пользе/эффективности лечебного воздействия
Класс IIb - польза / эффективность менее убедительны
Класс III - имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С |
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Классификация
Классификация: [
19
]
Полная транспозиция магистральных артерий (d-TMA) представляет собой аномалию вентрикуло-артериального соединения, при котором на фоне предсердного situs solitus аорта отходит от анатомически правого желудочка, а легочная артерия - от анатомически левого желудочка.
Классическую полную ТМС называют D-транспозицией, при которой аорта расположена спереди и справа от легочного ствола. Полная транспозиция магистральных артерий составляет 5-7 % всех ВПС; чаще она наблюдается улиц мужского пола (соотношение мужчин и женщин с данным пороком - 3:1)
В зависимости от сочетания ТМС с сопутствующими аномалиями выделяют четыре основных типа порока:
· Транспозиция магистральных артерий с интактной межжелудочковой перегородкой (простая транспозиция) (50%);
· Транспозиция магистральных артерий с ДМЖП;
· Транспозиция магистральных артерий с интактной МЖП/ДМЖП и ОВТЛЖ (КоА, перерыв дуги аорты);
· ТМС с ДМЖП и стенозом ЛА.
Классификация типов отхождения коронарных артерий:
Лейденская классификация коронарной анатомии при D-ТМС
Данная классификация определяет синусы аорты, от которых отходят три главные коронарные артерии. Два аортальных синуса Вальсальвы, прилежащие к аортолегочной перегородке, обращены к соответствующим синусам легочной артерии и в 99% случаев содержат устья коронарных артерий. Их называют «септальными» или «facing» (обращенные лицом) синусами.
Согласно конвенции, принято обозначать цифрами коронарные синусы:
· синус 1 - прилежащий к легочной артерии с левой стороны;
· синус 2 - прилежащий к легочной артерии с правой стороны.
Если магистральные артерии расположены в переднезадней проекции, септальные синусы направлены влево и вправо.
Если артерии расположены бок о бок, синусы направлены соответственно кпереди и кзади.
Если аорта расположена спереди и справа от легочной артерии (типичное взаимоотношение при ТМА), септальные синусы имеют переднелевое и заднеправое расположение.
Синус
Синус 1 - прилежащий к легочной артерии с правой стороны от наблюдателя;
Синус 2 - прилежащий к легочной артерии с левой стороны от наблюдателя.
Коронарные артерии:
Правая коронарная артерия (RСА);
Передняя нисходящая артерия (LAD);
Огибающая артерия (CX).
Буквой А обозначают отхождение большинства ветвей от общего сосуда, точкой с запятой (;) - отдельное отхождение.
ДОПОЛНИТЕЛЬНАЯ ОПИСАТЕЛЬНАЯ КЛАССИФИКАЦИЯ:
Прохождение главных ветвей коронарных артерий
По эпикарду:
· Переднее А: ветви проходят впереди аорты;
· Заднее А: ветви проходят позади легочной артерии;
· Между А: ветви проходят между магистральными артериями (обычно интрамурально).
Необычное отхождение:
· Комиссуральное А: коронарное устье располагается близко к комиссуре клапана;
· Раздельное: отдельные источники двух ветвей, от одного синуса аорты;
· Отдаленное или дистальное: отхождение огибающей и задней нисходящей артерии в качестве дистальной бифуркации правой коронарной артерии.
Расположение аорты относительно легочной артерии:
Справа или спереди, слева, «бок о бок», сзади.
Наиболее часто встречающийся вариант анатомии коронарных артерий; 1LCx2R
Показания к госпитализации: наличие врожденного порока сердца с нарушениями гемодинамики
Диагностика
Перечень основных и дополнительных диагностических мероприятий:
Основные (обязательные) диагностические обследования:
· определение суммарных антител к HBsAg вируса гепатита B в сыворотке крови ИФА-методом;
· определение суммарных антител к вирусу гепатита C в сыворотке крови ИФА-методом;
· исследование на возбудителя сальмонеллёза, дизентерии, брюшного тифа;
· бактериологическое исследование испражнений на патогенную и условно- патогенную микрофлору;
· исследование кала на яйца гельминтов;
· рентгенография органов грудной клетки в одной проекции;
· мазок из зева на патологическую флору
· микрореакция;
· исследование крови на ВИЧ;
· эхокардиография;
· ЭКГ;
· общий анализ мочи;
· общий анализ крови;
· биохимический анализ крови: (определение общего белка, глюкозы, креатинина, мочевины, АлТ, АсТ).
Дополнительные диагностические обследования:
· холтеровское мониторирование ЭКГ;
· электроэнцефалография;
· КТ и/или МРТ головного мозга;
· КТ и/или МРТ грудного, брюшного сегмента;
· УЗИ почек.
Эхокардиография:
Предсердно-желудочковая конкордантность и желудочково-артериальной дискордантность. ЭХО-признаки дискордантности:
· аорта отходит от ПЖ, легочная артерия от ЛЖ;
· магистральные сосуды и выводные тракты желудочков параллельны (выводятся одновременно без ротации датчика);
· полулунные клапаны расположены на одном уровне;
· митрально-легочное фиброзное продолжение (+);
· желудочки сердца расположены обычно, ПЖ гипертрофирован исследовании, дилатация ПЖ, различной степени, дилатация ЛА.
Задачи эхокардиографического исследования:
установить наличие дискордантных вентрикулоартериальных соотношений, пространственную ориентацию магистральных сосудов, отхождение проксимальных сегментов коронарных артерий, большинство важных сопутствующих аномалий, включая количество, размер и локализацию межкамерных коммуникаций (ООО, ОАП, ДМЖП), анатомический тип обструкции выводного тракта левого желудочка, аномалии AВ-клапанов, наличие пороков, обусловленных нарушением частей межжелудочковой перегородки и связанным с ней отхождением обоих магистральных сосудов от правого желудочка с подлегочным ДМЖП и нависающей легочной артерией.
Компьютерная ангиография/магнитно-резонансная томография: с целью диагностики анатомии порока и выявления сопутствующих ВПС.
Катетеризация полостей сердца : с целью проведения процедуры Рашкинда и диагностики сложных сопутствующих ВПС (обструкция ВОЛЖ). Катетеризацию проводят с измерением давления в левом желудочке, уточнения деталей анатомии порока и особенностей отхождения коронарных артерий, измерение давления в легочной артерии, что особенно важно при ТМС с ДМЖП и легочной сосудистой болезнью.
Показания для консультации специалистов
:
· Консультация аритмолога: наличие нарушений ритма сердца (пароксизмальная предсердная тахикардия, фибрилляция и трепетание предсердий, синдром слабости синусового узла), диагностированные клинически, по данным ЭКГ и ХМЭКГ.
· Консультация невропатолога: наличие эпизодов судорог, наличие парезов, гемипарезов и других неврологических нарушений;
· Консультация инфекциониста: наличие признаков инфекционного заболевания (выраженные катаральные явления, диарея, рвота, сыпь, изменение биохимических показателей крови, положительные результаты ИФА исследований на внутриутробные инфекции, маркеры гепатитов);
· Консультация оториноларинголога: носовые кровотечения, признаки инфекции верхних дыхательных путей, тонзиллиты, синуситы;
· Консультация гематолога: наличие анемии, тромбоцитоза, тромбоцитопении, нарушение свертываемости, другие отклонения гемостаза;
· Консультация нефролога: наличие данных за ИМВП, признаки почечной недостаточности, снижение диуреза, протеинурия.
Медицинский туризм
Пройти лечение в Корее, Израиле, Германии, США
Медицинский туризм
Получить консультацию по медтуризму
Лечение
Цель проведения процедуры/вмешательства:
· пациенты с подозрением на ТМС;
· хирургическое лечение патологической гемодинамики (восстановление нормальной гемодинамики);
· комплексное обследование;
· установление точного диагноза;
· определение критериев операбельности;
· выбор способа хирургического лечения;
· проведение операции, послеоперационное ведение.
Показание и противопоказание для проведения процедуры:
Показания для проведения процедуры/вмешательства:
· пациенты с диагностируемой транспозицией магистральных сосудов.
Противопоказание к проведению процедуры/вмешательства:
· гипоплазия системного (левого) желудочка, не устраненная предшествующим подготовительным этапом (суживания СЛА).
Требования к проведению процедуры/вмешательства:
Операции при ТМС осуществляется в хирургическом отделении или в центре, оснащенном в соответствии со стандартами оснащения отделений хирургического профиля, утвержденными в установленном порядке.
Требования к санитарно-противоэпидемическому режиму:
Меры безопасности и противоэпидемический режим согласно Санитарным правилам «Санитарно-эпидемиологические требования к объектам здравоохранения», утвержденным постановлением Правительства Республики Казахстан от 17 января 2012 года № 87.
Требования к оснащению:
Требования к основному перечню оснащения медицинской организации, в которой осуществляется операции по поводу ТМС
| N п/п | Наименование |
| 1 | Аппарат для гемодиализа и гемодиафильтрации |
| 2 | Аппарат искусственного кровообращения |
| 3 | Центрифужный насос крови |
| 4 | Молекулярно-адсорбирующая-циркулирующая система |
| 5 | Аппарат для экстракорпоральной мембранной оксигенации (ЭКМО) |
| 6 | Аппарат ультразвуковой диагностики экспертного класса с доплером |
| 7 | Компьютерный томограф |
| 8 | Магнитно-резонансный томограф |
| 9 | Ангиограф |
| 10 | Система для очистки и аутотрансфузии крови |
| 11 | Аппарат рентгеновский стационарный |
| 12 | Мобильная рентгенографическая система |
Требования к расходным материалам:
Стерильные разовые расходные материалы:
· канюли для проведения ИК;
· нити синтетические монофиламентные;
· нити с покрытием из полимера (этилен терефталат);
· многонитчатый шовный материал из синтетического сополимера, состоящего на 90% из гликолида и на 10% из L-лактида, титановая проволока.
Отдельные формы ТМС требуют:
· биологические клапансодержащие кондуиты.
Требования к лекарственным средствам:
Медикаментозное лечение: Внутривенная инфузия препаратов простагландина Е 1 с целью препятствования закрытия ОАП.
· коррекция метаболического ацидоза;
· коррекция гипогликемии;
· коррекция гипокальциемии.
Медикаментозное лечение
:
На первом этапе проводится постоянная инфузия простагландина E1 (из расчета 0,01 - 0,04 мкг/кг/мин) для предупреждения закрытия артериального протока. Это особенно важно при ТМС с ДМЖП и обструкцией выводного тракта левого желудочка. Во время катетеризации сердца у новорожденных с выраженной гипоксемией проводится баллонная атриосептостомия Рашкинда.
Эффективной считают процедуру, после которой сатурация повысилась на 10% и более и не развивается метаболиче-ский ацидоз. Косвенными признаками успешной процедуры являют-ся: увеличение потока через межпредсердное сообщение, определяе-мое с помощью цветной допплерографии, появление флотирующих кра-ев перегородки в области отверстия, изменение относительных разме-ров предсердий.
Проводится коррекция метаболического ацидоза бикарбонатом натрия.
При развитии отека легкого и тяжелой гипоксемии при необходимости больной переводится на искусственную вентиляцию легких.
В случаях ригидной межпредсердной перегородки возможно при-менение ножевой атриосептостомии или дилатации отверстия балло-ном высокого давления.
Следует отметить, что активное применение простагландинов в условиях малого межпредсердного сообщения может быть опасным. Это связано с тем, что большой сброс через ОАП, приводящий к уве-личенному возврату крови из легких в левое предсердие, сопровожда-ется неадекватным опорожнением последнего и чревато развитием оте-ка легких.
Мероприятия, направленные на купирование симптомов недостаточности кровообращения: нормализация сердечного выброса:
Диуретики:
при недостаточности кровообращения - фуросемид 1-3 мг/кг/сут в 3 приема с переходом на триамтерен 1-3 мг/кг/сут или верошпирон 2-4 мг/кг/сут;
Сердечные гликозиды:
при наличии недостаточности кровообращения 2-ой и более степени - дигоксин в поддерживающей дозе 0,006-0,008 мг/кг/сут в 2 приема через 12 часов;
Ингибиторы ангиотензин-превращаюшего фермента:
снижение периферического тонуса, уменьшение постнагрузки:
· каптоприл 0,05 - 0,5 мг/кг/сут детям младше 6 месяцев, детям старше 6 месяцев 0,5-2,0 мг/кг/сут в 3 приема;
· эналаприл (энам) 0,1-0,5 мг/кг/сут в 2 приема.
Антибактериальная терапия:
с учетом интеркуррентных заболеваний, застойной пневмонии (предпочтительно назначение цефалоспоринов 2 - 3 поколения, возможно назначение в сочетании с аминогликозидами) с последующим переходом на пероральную антибактериальную терапию.
В тяжелых случаях использование антибиотиков резерва: имипенем, карбипенем, ванкомицин, ципрофлоксацины, макролиды.
«Защищенные» пенициллины (амоксиклав, аугментин из расчета 20-50 мг/кг сутки) в 2-3 приема перорально;
Макролиды: спирамицин 1,5 млн Е./10 кг/сутки - 2 раза в день; сумамед в суточной дозировке 10 мг/кг в 1 день приема, 5 мг/кг со 2 по 5-ый день приема, курсом 3-5 дня);
Цефалоспорины
II
-
III
поколения
в суточной дозе 70-100 мг/кг сутки (цефуроксим, цефтазидим, цефтриаксон, цефаперазон, цефотаксим) - 2 раза в день в/в, в/м;
«защищенные цефалоспорины» - сульфперазон 20-40 мг/кг;
Цефалоспорины
IV
-го поколения
- максипим - 70- 100 мг/кг в сутки - 2 приема, в/в или в/м;
Аминогликозиды : гентамицин 2-4 мг/кг в сутки в 2 приема, предпочтительно в/м не более 7 дней, амикацин 10-15 мг/кг в сутки в 2 приема в/м иди в/в - под контролем диуреза, уровня мочевины, креатинина в крови, мониторинг слуха;
Карбопенемы: меропенем- 15-20 мг/кг - 3-4 раза в сутки в/в струйно или капельно, тиенам - 15-20 мг/кг в сутки каждые 6-8 часов в/в струйно и капельно;
Гликопептиды: (Ванкомицин) 15-30 мг/кг.
Основные лекарственные препараты, применяемые при лечение новорожденных с транспозицией магистральных сосудов:
| № |
название препарата |
форма выпуска |
дозировка |
длительность применения |
| 1 | Вазодилататоры: | |||
| Алпростадил |
лиофилизат для приготовления инфузионного раствора, 1 ампула - 20 мкг |
0,01 - 0,1 мкг/кг/мин, путем титрования |
10 дней | |
|
0,1 - 0,2 мкг/кг/мин путем титрования по строгим показаниям (фармакологическая реканализация ОАП |
||||
| 2. | Кардиотонические препараты: | |||
|
Добутамина гидрохлорид |
раствор для инфузий, 1 флакон 50 мл/250 мг |
5-15 мкг/кг/мин | 10 дней | |
|
допамина гидрохлорид |
Концентрат для приготовления раствора для инфузий 1 мл/ 5 мг 1 ампула - 5 мл |
2-20 мкг/кг/мин | 10 дней | |
| 3. | Мочегонные средства | |||
| фуросемид | 1 ампула 10 мг |
0,5 - 1 мг/кг разовая доза 3-4 раза в сутки |
10 дней | |
| спиронолактон | 1 т. 25 мг | 2-4 мг/кг/сутки | 10 дней | |
| 4. | Ингибиторы АПФ | |||
| каптоприл | 1 т. 25 мг |
0,1-0,5 мг/кг/сутки |
10 дней | |
| эналаприл | 1 т. 2,5 мг |
0,1 - 0,5 мг/кг/сутки |
10 дней | |
| 5. | блокаторы адренорецепторов | |||
| карведилол | 1 т. 6,25 мг |
0,1 -0,8 мг/кг/сутки |
10 дней | |
| пропранолол | 1 т. 10 мг | 1 мг/кг/сутки | 10 дней | |
| 6. | Сердечные гликозиды | |||
| дигоксин | 1 т. 250 мкг |
дозировки представлены в таблице № 5 |
10 дней | |
| 7. | растворы для внутривенных инфузий | |||
| натрия хлорид 0,9% |
раствор для инфузий, 1 фл. - 100 мл, 200 мл |
10 мл/кг | 10 дней | |
|
глюкоза раствор для инфузий 5%, 10% |
1 флакон -100 мл 200 мл |
10 мл/кг | 10 дней | |
|
натрия гидрокарбонат 4% |
раствор для инъекций, 1 ампула - 20 мл |
дозировка по результатам КЩС крови |
по потребности |
|
| 4. | Антибактериальные препараты | ||
| Цефазолин |
100 мг/кг в сутки В 2-4 приема в/в |
10 дней | |
| Цефуроксим | 100 мг/кг в сутки в 2-4 приема в/в | 10 дней | |
| Фортум | 100 мг/кг/сутки | 10 дней | |
| Амикацин |
10-15 мг/кг/сутки В 2 введения в/в |
7-10 дней | |
| 5. | Диуретики | ||
| Фуросемид |
0,5 - 1 мг/кг разовая доза 3-4 раза в сутки |
14 дней | |
| Верошпирон |
2-4 мг/кг в сутки в 2 приема перорально в 8.00, в 12.00 |
14 дней | |
| 6. | Ингибиторы АПФ | ||
| капотен 1 т. 25 мг |
0,1-0,5 мг/кг в сутки в 3 приема |
14 дней | |
| энап 1 т. 2,5 мг |
0,1-0,5 мг/кг/ сутки |
14 дней | |
| 7. | блокаторы - β-адренорецепторов | ||
| карведилол |
0,1-0,8 мг/кг в сутки в 2 приема |
14 дней | |
| анаприлин | 1 мг/кг/сутки в 3 приема | 14 дней | |
| метопролол | 5 мг/кг/сутки в 2 приема | 14 дней | |
| 8. |
Растворы для в/венных инфузий |
||
| Физ. Р-р | 10 мл/кг | 14 дней | |
| Глюкоза 10% | 10 мл/кг | 14 дней | |
| Аминоплазмаль | 14 дней; | ||
| Гидрокарбонат натрия |
Расчет на основании показателей КЩС |
По потребности |
Требования к соблюдению мер безопасности:
· идентификация пациента.
Требования к подготовке пациента:
Письменное информированное согласие пациента на проведение процедуры;
В виду сложности порока пациенты с диагнозом ТМС без дефекта межжелудочковой перегородки в дооперационном периоде должны находится в ОАРИТ. Пациенты с ТМС и дефектом межжелудочковой перегородки с хорошим сбросом на уровне дефекта - пребывание в дооперационном периоде возможно в отделение кардиохирургии в случае стабильного исходного состояния.
Непосредственная предоперационная подготовка:
Возможна госпитализация
,
как в плановом порядке, так и по линии санитарной авиации.
· прекращение приема пищи и жидкости (не менее 6 часов до начала операции);
· установка внутрисосудистых катетеров.
Анестезиологическое пособие
:
· премедикация проводится с учетом основного заболевания;
· мониторинг состояния пациента: ЭКГ (3 отведений), HR, SpO2, IBP, CVP, пульсоксиметрия, температура пациента; капнография, чрезпищеводная эхокардиография); церебральная оксиметрия.
· вводный наркоз/индукция:
- наркотические анальгетики (фентанил 5-10 мкг/кг в/в);
- седативные препараты (диазепам0,3-0,5 мг/кг в/в);
-миорелаканты (аркурон 0,08 мг/кг в/в);
- после введения миорелаксантов;
· интубация трахеи выполняется трубкой в зависимости от возраста и особенности верхних дыхательных путей. Контроль положения трубки может выполнятся клинический - аускультация и фибробронхоскопия - «золотой стандарт».
· базовый наркоз: наркотические анальгетики (фентанил 10-15 мкг/кг/час в/в на титровании), ингаляционный анестетик (севофлуран), низкопоточная анестезия до 2 л/мин.
· Во время операции - пропофол 3-8 мг/кг/ч в\в, миорелаксация - аркурон 0,08 мг/кг в/в каждые 60-90 мин.
Препараты выбора для наркоза:
- фентанил 5-10 мкг/кг в/в
- изофлуран и десфлуран
- аркурон 0,08 мг/кг в/в каждые 60-90 мин.
· режим ИВЛ направлен на нормализацию газового состава крови: нормовентиляция, дыхательный объем - 6-8 мл/кг идеальной массы тела, I:E/1:2, ПДКВ - 5-7 см.вод.ст, с повышением FiO2 - 80-100% на начальном этапе операции, капнография - нормокапния;
· инфузионная терапия направлена на поддержание адекватной волемии, достаточного коллоидного давления плазмы, восполнение потери эритроцитов, факторов свертывания и тромбоцитов: препараты крови - эритроцитарная масса 5-20 мл/кг, СЗП 5-20 мл/кг мл, концентрат тромбоцитов 1-2 дозы.
· целевые значения Нв не менее 130 г/л, кристаллоидные растворы, применение коллоидных растворов возможно при гиповолемии под контролем центрального венозного давления;
Основной этап операции
проводится в условиях искусственного кровообращения.
Канюляция: центральная
Гепарин 300 ед/кг перед канюляцией для ИК, контроль АВС во время работы ИК.
Кардиотоническая поддержка инотропными препаратами:
· норэпинефрин 0,02- 0,5 мкг/кг/мин;
· эпинефрин 0,02- 0,3 мкг/кг\мин;
· дофамин 3-15 мкг/кг/мин;
· добутамин 3-15 мкг/кг/мин;
· милринон 0,1-0,5 мкг/кг/мин;
· симдакс 0,2 мкг/кг/мин;
· фенилэфрин.
После завершения хирургического гемостаза производится нейтрализация гепарина протамин-сульфатом под контролем активированного времени свертывания. Ингибиторы фибринолиза (транексамовая кислота).
Инфузия свежезамороженной плазмы (5-20 мл/кг), криопреципитата, тромбомассы, крововозамещение свежей эритроцитарной массой осуществляется строго по показаниям (согласно Приказу № 666 Министерства здравоохранения РК "Об утверждении Номенклатуры, Правил заготовки, переработки, хранения, реализации крови и ее компонентов, а также Правил хранения, переливания крови, ее компонентов и препаратов" и приложения к нему).
Лечение когулопатических кровотечений:
Октаплекс
0,9-1,9 мл/кг, максимальная разовая доза 500 МЕ (20 мл Октаплекса). Расчет необходимой дозы для лечения является в основном эмпирическим, из расчета, что 1МЕ фактора II или фактора Х на 1 кг/массы тела, соответственно, увеличивает активность плазменного фактора II или Хна 0,02 и 0,017 МЕ/мл.
Эптаког альфа
: начальная доза 90 мкг/кг, которая вводится через 2 ч, а затем препарат вводится с 2-3-часовыми интервалами на протяжении первых 24-48 ч в зависимости от проводимого вмешательства и клинического состояния пациента.
Лечение легочной гипертензии:
· монооксид азота 10-40 ppm под контролем тромбоцитов и метHb;
· илопрост ингаляции 2,5-10 мкг 4 раза в день.
Антибиотикопрофилактика:
Антибактериальные средства.
Цефалоспорины II, III поколения в качестве базовой антибиотикотерапии. Карбопенемы назначаются в зависимости от результатов бактериальных посевов пациента.
Антимикотики:
· Амфотерицин В липидный комплекс, ингаляционно, через небулайзер, 50 мг/сут для экстубированных пациентов, 100 мг/сут для интубированных пациентов. В течении 4 дней после трансплантации, далее по потребности.
· Нистатин, суспензия, 100 тыс. ед/мл, 5 мл 4 раза в день, 6 мес. после трансплантации.
· Вориконазол 6 мг/кг, в/в (или 400 мг peros), каждые 12 часов, далее 4 мг/кг в/в (или 200 мг peros), каждые 12 часов, в течении 4 мес. после трансплантации.
Методика проведения процедуры/вмешательства: (см. Приложение 1)
Эндоваскулярная баллонная атриальная септостомия -
паллиативный метод лечения в случае абсолютных противопоказаний по сопутствующей патологии и как метод стабилизации состояния ребенка перед радикальной хирургической операцией.
Баллонная атриальная септостомия (процедура Рашкинда):
показана, если имеется рестриктивный ДМПП при следующей патологии:
- ТС с интактной межжелудочковой перегородкой (класс
I
);
- ТМС в сочетании с ДМЖП/ОАП, если хирургическая коррекция откладывается на несколько недель в силу объективных причин (класс
I
), (градиент давления между предсердиями более 6 мм рт.ст. - рестриктивная коммуникация) хирургическая коррекция, как наиболее традиционный метод.
Виды хирургической коррекции:
Одноэтапная коррекция
· ТМС с интактной МЖП - операция артериального переключения;
· ТМС с ДМЖП - операция артериального переключения + пластика дефекта заплатой из аутоперикарда/ксеноперикарда/синтетической заплатой;
· ТМС с ДМЖП и стенозом ЛА - операция Растелли, REV, операция Никайдо
· ТМС с ОВТЛЖ (КоА, перерыв дуги аорты)- реконструкция дуги аорты с артериальным переключением.
Двухэтапная коррекция включает в себя:
Сужение легочной артерии (операция Мюллера, бэндинг) в сочетании с наложением модифицированного системно-легочного анастомоза/ атриосептостомии. Показана при инволюции миокарда ЛЖ в целях подготовки ЛЖ для дальнейшей системной циркуляции.
Причины отсрочки операции за пределы «безопасного» для артериального переключения периода:
· возраст старше 4-8 недель, если давление в ЛЖ составляет менее 66% от системного давления, отношение массы левого желудочка к массе правого желудочка < 0,6/;
· пациенты с ТМА с ИМЖП в возрасте до 3 недель с гипоплазией левого желудочка;
· некротический энтероколит;
· почечная и печеночная недостаточность;
· кровоизлияние в мозг;
· сепсис, недоношенность с очень малой массой ребенка;
· ожидаемое спонтанное закрытие ДМЖП;
· поздняя постановка диагноза;
· после неудачной коррекцией ТМС на уровне предсердий (после операций предсердного переключения по методикам Мастарда или Сеннинга).
В этих случаях есть выбор между первичной коррекцией гемодинамики на предсердном уровне и двухэтапным анатомическим хирургическим лечением.
Дополнительными полезными, но не решающими критериями являются эхокардиографические показатели - наличие или отсутствие выбухания межжелудочковой перегородки в полость левого желудочка, толщина стенки, объем желудочка.
Эхокардиография:
критерии готовности пациента к радикальной коррекции ТМС в поздние сроки обращения/выявления:
· Индекс КДО ЛЖ (характеризует степень гипоплазии полости желудочка. Нижняя граница нормы 35 мл/м 2);
· Индекс толщины задней стенки ЛЖ в диастолу (косвенно отражает степень увеличения давления в ЛЖ;
· Нормальный индекс толщины стенки ЛЖ -13-17 мм/м 2);
· Индекс массы миокарда ЛЖ (характеризует степень гипертрофии и гипоплазии ЛЖ. Нормальный индекс массы миокарда ЛЖ - не менее 34-35 гр/м 2);
· Индекс давления ЛЖ/ПЖ (отражает степень повышения давления в ЛА и ЛЖ и достаточность нагрузки на ЛЖ для поддержания системного кровообращения после анатомической коррекции;
· Допустимые значения - > 0,5-0,6 /Castaneda А.).
· Индекс формы ЛЖ (характеризует геометрию ЛЖ (отношение передне-заднего размера ЛЖ к боковому в фазу систолы) LosayJ., PlancheC., Lacour-GayetF. (2002 г.):А. 1,0 - 1,5В. 1,5 - 2,5С. > 2,5

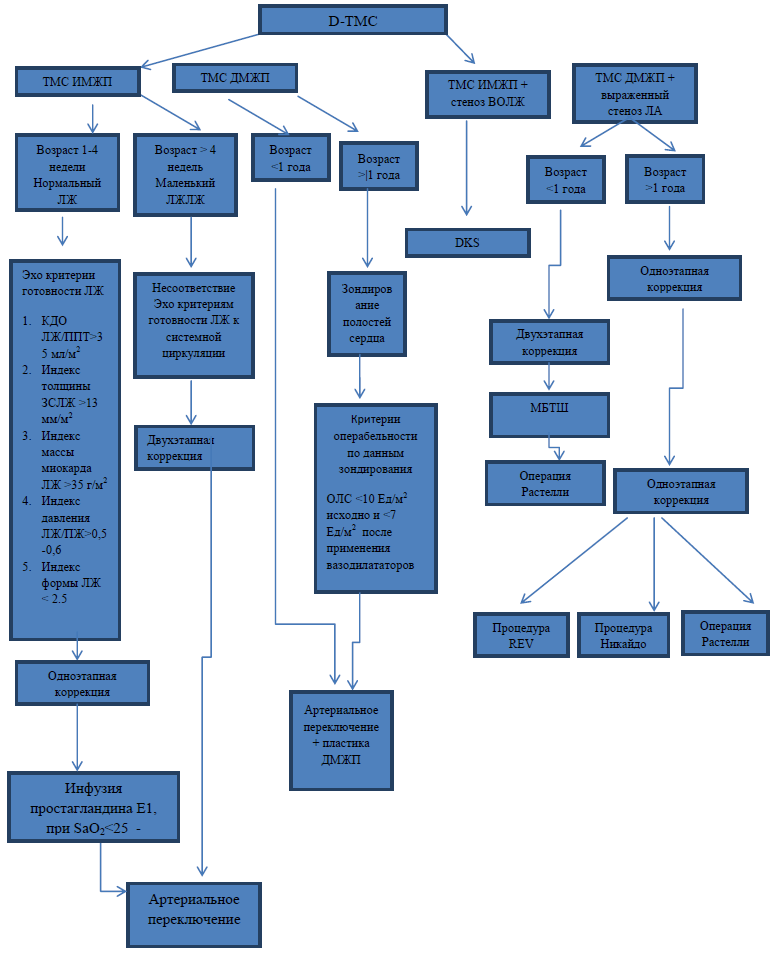
Хирургическая тактика и сроки оперативной коррекции
(Алгоритм принятия решений)
Младенцы с простой формой ТМС (с ИМЖП)
· Артериальное переключение является операцией выбора, оптимальное время ее выполнения в первые 2 недели жизни, но не позже 4-недельного возраста. Ранняя хирургическая летальность в клиниках, имеющих опыт, составляет 2-5%.
· Суммарная 5 летняя выживаемость в среднем равна 85%.
· Если сроки артериального переключения упущены (т.е. после месячного возраста), может быть предпринято двухэтапное лечение. Оно предполагает суживание легочной артерии с межартериальным шунтом или без него и затем.
· Артериальное переключение.
· Детям с неблагоприятной анатомией коронарных артерий выполняют операцию переключения на предсердном уровне (операции Сеннинга или Mастард) в возрасте 3-9 мес. или артериальное переключение при достаточном опыте выполнения этих операций.
Младенцы с ОАП.
При наличии небольшого ОАП тактика та же, что и при ИМЖП. При большом ОАП, протекающем с сердечной недостаточностью, сроки операции могут быть удлинены до 2-3 недель. Риск летального исхода не превышает 5%.
ТМС с изолированным СЛА.
· Динамическая обструкция выводного тракта левого желудочка не препятствует выполнению артериального переключения. Этот тип обструкции разрешается спонтанно после операции.
· Невыраженный анатомический клапанный или подклапанный стеноз устраняется во время операции артериального переключения без увеличения хирургического риска.
· При наличии выраженного СЛА оптимальным вмешательством является операция Senning хирургическое устранение стеноза в 3-6месячном возрасте.
ТМС с ДМЖП.
· При небольшом ДМЖП тактика та же, что и при простой ТМА.
· При наличии большого ДМЖП наиболее распространенной практикой является операция артериального переключения с одновременным закрытием ДМЖП без предшествующего суживания легочной артерии в возрасте 2 недели - 2 месяцев. Риск операции при этом не повышается. Допустимым, но не лучшим методом является операция Senning с одновременным закрытием ДМЖП без суживания легочной артерии в возрасте 3 - 4 мес.
· Множественный ДМЖП представляет особую, редко встречающуюся патологию. Этим пациентам показано суживание легочной артерии к 3 - 4 месяцев жизни, в более позднем периоде - операция Фонтен.
· Больным с большим ДМЖП и сопутствующим субаортальным стенозом показана операция артериального переключения с резекцией элементов подклапанного сужения. При диффузной гипоплазии выводного тракта правого желудочка и клапанного кольца аорты показана операция Дамус-Кей-Стэнсел в сочетании с Растеллив возрасте 1-2 года. Летальность составляет 15-30%.
· При гипоплазии дуги и коарктации аорты предпочтительнее одномоментная реконструкция аорты и артериальное переключение.
· Больным с большим ДМЖП и гипоплазированным правым желудочком или «верхом сидящим» АВ клапаном не может быть выполнена ни одна из приведенных выше операций, так как в первом случае анатомия порока соответствует функционально единственному желудочку сердца, а во втором — разделение левых и правых отделов сердца технически невозможно. Для этого варианта показано раннее суживание легочной артерии и позднее - операция Фонтен.
ТМС в сочетании с ДМЖП и СЛА.
· При умеренном стенозе легочной артерии тактика та же, что и при изолированном большом ДМЖП. Может быть также применена коррекция по Сеннинг в 3-9месячном возрасте.
· При выраженном СЛА с большим ДМЖП в период новорожденности может в случаях выраженного цианоза потребоваться наложение системно-легочного анастомоза. В 3-5летнем возрасте выполняют операцию Rastelli. Современным стандартом риска при этой операции является летальность около 5%. При неблагоприятных условиях вместо анатомической может быть выполнена гемодинамическая коррекция по Fontan в возрасте 2-4 года.
· Альтернативой операции Растелли, позволяющей избежать применения экстракардиального кондуита, является операция Лекомпт (REV). Операция состоит из следующих основных моментов: резекция инфундибулума для расширения ДМЖП, внутрижелудочковый тоннель, для перенаправления потока из левого желудочка к аорте, пересечение аорты для выполнения маневра Лекомпт и прямая реконструкция легочной артерии к правому желудочку с использованием заплаты по передней поверхногсти. Ее выполняют в возрасте 6 мес. - 5 лет с той же степенью хирургического риска, что и операцию
· Операция Растелли состоит из следующих основных моментов: поток из левого желудочка через внутрижелудочковый тоннель направляется в аорту и восстанавливается сообщение правый желудочек - легочная артерия с помощью клапансодержащего кондуита. Внесердечная часть операции состоит в транслокации отсеченного легочного ствола на переднюю стенку правого желудочка. Этот маневр в зависимости от расположения легочного ствола выполняют с пересечением восходящей аорты (как при операции артериального переключения) или без него.
· Операция Никайдо, которая предусматривает перемещение устья аорты с селективным индивидуальным перемещением коронарных артерий и бивентрикулярную реконструкцию выводного тракта, предложена для транспозиции со СЛА.
Уровень сложности по базовой шкале Аристотеля:
|
Процедура/ операция |
Сумма балов (базовая шкала) | Уровень сложности | Смертность | Риск осложнений |
Сложность |
|
сосудов |
10.0 | 4 | 3.5 | 3.0 | 3.5 |
|
Операция артериального переключения при транспозиции магистральных сосудов в сочетании с пластикой дефекта межжелудочковой перегородки |
11.0 | 4 | 4.0 | 3.0 | 4.0 |
|
Формирование модифицированного системно-легочного анастомоза по Блэлок-Тауссиг |
6.3 | 2 | 2.0 | 2.0 | 2.3 |
| Операция Сеннинга | 8.5 | 3 | 3.0 | 2.5 | 3.0 |
| Операция Мастарда | 9.0 | 3 | 3.0 | 3.0 | 3.0 |
| Операция Растелли | 10.0 | 4 | 3.0 | 3.0 | 4.0 |
| Процедура REV (reparation a l"etageventriculaire) | 11.0 | 4 | 4.0 | 3.0 | 4.0 |
| Операция Nikaidoh (Никайдо) | |||||
|
Процедура Дамус-Кей-Стэнсел |
9.5 | 3 | 3.0 | 3.0 | 3.5 |
| Бэндинг легочной артерии | 6.0 | 2 | 2.0 | 2.0 | 2.0 |
|
Создание/ увеличение дефекта межпредсердной перегородки |
4.0 | 1 | 1.0 | 2.0 | 1.0 |
Значимость баллов по базовой шкале Аристотеля
|
Баллы БША |
Смертность |
Риск осложнений. Длительность пребывания в ОИТ |
Сложность |
| 1 | <1% | 0-24часов | Элементарная |
| 2 | 1-5% | 1-3 дней | Простая |
| 3 | 5-10% | 4-7 дней | Средняя |
| 4 | 10-20% | 1-2 недели | Существенная |
| 5 | >20% | >2 недель | Повышенная |
Послеоперационное наблюдение:
Длительность наблюдения пациентов прооперированных по поводу ТМС пожизненная с интервалом 6-12 мес.
Цель наблюдения
: диагностика возможных осложнений в отдаленном послеоперационном периоде. При развитии того или иного осложнения решение о виде лечения принимается в индивидуальном порядке.
Профилактика бактериального эндокардита проводится по показаниям в первые 6 месяцев после хирургической коррекции порока или более в случае наличия резидуальных шунтов в МЖП.
В случае регистрации в послеоперационном периоде непродолжительной преходящей атриовентрикулярной блокады необходимо длительное наблюдение без ограничения сроков (ЭКГ 1 раз в 6 месяцев, ХМЭКГ 1 раз в год).
Наиболее частые проблемы раннего послеоперационного периода при коррекции ТМС:
· наличие резидуального сброса;
· нарастание сердечной недостаточности;
· артериальная гипертензия;
· нарушение ритма сердца и атриовентрикулярной проводимости (пароксизмальная предсердная тахикардия, фибрилляция и трепетание предсердий, синдром слабости синусового узла);
· повреждение возвратного гортанного нерва (чаще при «неудобном расположении» протока).
· повреждение диафрагмального нерва.
· хилоторакс (возникает в результате повреждения грудного протока). Лечение включает в себя дренирование грудной полости.
· постперикардиотомный синдром (перикардит);
· экссудативный перикардит.
· инфекционные осложнения: госпитальная пневмония, инфекция раны, бактериальный эндокардит, активизация хронической инфекции, в том числе вызванной внутриклеточными возбудителями (хламидии, микоплазмы, ЦМВ, ВПГ).
· инфекционный эндокардит;
· неврологические нарушения: энцефалопатия, судорожный синдром.
Поздние осложнения:
| Атриальное переключение | Артериальное переключение | Операция Растелли |
| Обструкция легочного (5%) и системного (5%) венозного возврата | Обструкция ВОПЖ (надклапанная или на уровне ветвей ЛА), суправентрикулярный стеноз аорты | Обструкция на уровне кондуита ПЖ-ЛА (неизбежно) |
| Остаточный шунт на предсердном уровне (20%) | Регургитация на неоаортальном клапане | Значительная субаортальная обструкция (через ДМЖП и аорто-левожелудочковый тоннель) |
| Недостаточность трехстворчатого клапана в отдаленные сроки после операции (40%) | Миокардиальная ишемия | Резидуальный ДМЖП |
| Отсутствие синусового ритма (более 50%) | Эндокардит | Дисфункция ПЖ / ЛЖ |
| Частая суправентрикулярная аритмия | инфаркт, дисфункции желудочков, регургитация на полулунных клапанах. | Предсердные, желудочковые аритмии |
| Сниженная толерантность правого желудочка (системного желудочка) к физической нагрузке. Дисфункция системного ПЖ | Внезапная смерть | |
| Обструкция оттока по ВПВ, НПВ | Полная АВ блокада | |
| Внезапная смерть, обусловленная нарушением ритма (3%) | Эндокардит | |
| Эндокардит | ||
| Обструктивная болезнь легочных сосудов. | ||
| Перечисленные осложнения в большей степени характерны для операции Mustard |
Индикаторы эффективности процедуры/вмешательства:
Результат считается хорошим, если клинически ребенок чувствует себя удовлетворительно, аускультативно отсутствует шумовая симптоматика, по данным ЭХОКГ-нет градиента на неоаорте, неолегочной артерии, хорошей сократительная способность миокарда, в случае сопутствующего ДМЖП-заплата герметична, нет жидкости в перикарде, плевральных полостях. Рана заживает первичным натяжением.
Результат считается удовлетворительным при наличии удовлетворительного самочувствия ребенка, аускультативно незначительного систолического шума по левому краю грудины, по данным ЭХОКГ - имеетсягемодинамически не значимый градиент на неоаорте, неолегочной артерии, в случае сопутствующего дмжпрезидуальный дефект допустимых размеров, с высоким чрежжелудочковым градиентом, удовлетворительной сократительной способности миокарда, нет жидкости в перикарде, плевральных полостях.
Результат считается неудовлетворительным при сохраняющейся клиники сердечной недостаточности. Аускультативно - глухость тонов, систолический шум по левому краю грудины, по данным ЭХОКГ - имеется гемодинамически значимый градиент на неоаорте, неолегочной артерии, низкой сократительной способностью миокарда, в случае сопутствующего ДМЖП имеется резидуальный дефект с большим лево-правым шунтом, с низким чрежжелудочковым градиентом, наличие жидкости в перикарде, плевральных полостях. Показана повторная операция.
Препараты (действующие вещества), применяющиеся при лечении
| Алпростадил (Alprostadil) |
| Амикацин (Amikacin) |
| Аминокислоты для парентерального питания + Прочие препараты (Минералы) (Aminoacids for parenteral nutrition + Other medicines (Multimineral)) |
| Амфотерицин B (Amphotericin B) |
| Вориконазол (Voriconazole) |
| Гепарин натрия (Heparin sodium) |
| Декстроза (Dextrose) |
| Десфлуран (Desflurane) |
| Дигоксин (Digoxin) |
| Добутамин (Dobutamine) |
| Допамин (Dopamine) |
| Изофлуран (Isoflurane) |
| Илопрост (Iloprost) |
| Каптоприл (Captopril) |
| Карведилол (Carvedilol) |
| Концентрат тромбоцитов (КТ) |
| Криопреципитат |
| Левосимендан (Levosimendan) |
| Метопролол (Metoprolol) |
| Милринон (Milrinone) |
| Монооксид азота |
| Натрия гидрокарбонат (Sodium hydrocarbonate) |
| Натрия хлорид (Sodium chloride) |
| Нистатин (Nystatin) |
| Норэпинефрин (Norepinephrine) |
| Пипекурония бромид (Pipekuroniyu bromide) |
| Плазма свежезамороженная |
| Пропранолол (Propranolol) |
| Спиронолактон (Spironolactone) |
| Транексамовая кислота (Tranexamic acid) |
| Факторы свертывания крови II, VII, IX и X в комбинации Протромбиновый комплекс) (Coagulation Factor II, VII, IX and X in combination (Prothrombin complex)) |
| Фенилэфрин (Phenylephrine) |
| Фентанил (Fentanyl) |
| Фуросемид (Furosemide) |
| Цефазолин (Cefazolin) |
| Цефтазидим (Ceftazidime) |
| Цефуроксим (Cefuroxime) |
| Эналаприл (Enalapril) |
| Эналаприлат (Enalaprilat) |
| Эпинефрин (Epinephrine) |
| Эптаког альфа (активированный): рекомбинантный коагуляционный фактор VIIa (Eptakog alfa (activated, 1); recombinant coagulation factor VIIa) |
| Эритроцитарная масса |
Группы препаратов согласно АТХ, применяющиеся при лечении
Информация
Источники и литература
- Протоколы заседаний Экспертного совета РЦРЗ МЗСР РК, 2015
- Список использованной литературы: 1. «Детская кардиология». Под редакцией Белозерова Ю.М.. Москва «МЕДпрессинформ» 2004 г. 2. Guidelines Consensus on Timing of Intervention for Common Congenital Heart Diseases. Indian Pediatrics 2008; 45: 117-126 3. INTRODUCTION TO CONGENITAL HEART DISEASE Duncan G. de Souza MD, FRCPC Clinical Assistant Professor Department of Anesthesiology and Pharmacology University of British Columbia Vancouver, British Columbia 2008 4. Врожденные пороки сердца. Справочник для врачей. Кривощеков Е.В., Ковалев И.А., Шипулин В.М. Томск 2009 5. Зиньковский М.Ф. Врожденные пороки сердца/Под ред. А.Ф. Возианова. - К.: Книга плюс, 2008. –1168 с.: ил. 6. Kirklin JW, Blackstone EH, Tchervenkov CI, Castaneda AR, and The Congenital Heart Surgeons Society. Clinical outcomes after the arterial switch operation for transposition. Patient, support,procedural, and institutional risk factors. Circulation 1992;86:1501 7. Lavoie J., Burrows FA., Hansen D.D. Video-assisted thoracoscopic surgery for the treatment of congenital cardiac defects in the pediatric population // Anesth. Analg.-1996.-82 (3).-P.563-567. 8. Liu H.P., Chang C.H., Lin P.J., Hsieh H. C, Chang J.P., Hsieh M.J. Thoracoscopic management of effusive pericardial disease: indications and technique // Ann. Thorac. Surg.-1994.-58 (6).-P. 1695-1697 Lupoglazoff J.M., Laborde F., Magnier S., Casasoprana A. Closure of patent ductus 9. Jonas RA, Giglia TM, Sanders S, et al. Rapid, two_stage arterial switch fo transposition of the great arteries and intact ventricular septum beyond the neonatal period. Circulation 80(suppl I):203, 1989. 10. Castaneda AR, Norwood WI, Jonas RA, еt al: Transposition of the great arteries and intact ventricular septum: Anatomical repair in the neonate. Ann Thorac Surg 38:438-443, 1984. 11. Lecompte Y, Zannini L, Hazan E et al. Anatomic correction of transposition of the great arteries. A new technique without use of prosthetic conduit. J Thorac Cardiovasc Surg 82:629, 1981. 12. Damus PS. Letter to the editor. Ann Thorac Surg 20:724, 1975. 13. Kaye MP. Anatomic correction of transposition of the great arteries. Mayo Clin Proc 50:638, 1975. 14. Stansel HC Jr. A new operation for D_loop transposition of the great vessels. Ann Thorac Surg 19:565, 1975. 15. Castaneda AR, Jonas RA, Mayer JE, Hanley FL. Cardiac surgery of the Neonate and Infant, WB Saunders company, Philadelphia, 1994. 16. Lock J, Lucas RV Jr, Amplatz K, Bessinger FB Jr. Silent unilateral pulmonary venous obstruction: occurrence after surgical correction of transposition of the great arteries. Chest 197S;73:224-227. 17. Wernovsky C, Giglia TM, Jonas RA, Mone SM, Colan SD, Wessel DL. Course in the intensive care unit following "preparatory" pulmonary artery banding and aortopulmonary shunt placement for transposition of the great arteries with low left ventricular pressure. Circulation 1992:86(suppl 2):133-139. 18. Leibman J, Cullum L, Belloc NB. Natural history of transposition of the great arteries - anatomy and birth and death characteristics.Circulation 1969;40:237-262). 19. Зиньковский М.Ф. Врожденные пороки сердца, 2008. –1168 с. 20. Blalock A, Hanlon C: The surgical treatment of complete transposition of the aorta and the pulmonary artery. Surg Gynecol Obstet 90:1, 1950. 21. Barratt_Boyes BG: Cardiac surgery in neonates and infants. Circulation 44:924- 925, 1971.
Информация
Список разработчиков протокола:
1) Горбунов Дмитрий Валерьевич - кандидат медицинских наук АО «Национальный научный кардиохирургический центр» заведующий детским кардиохирургическим отделением.
2) Иванова-Разумова Татьяна Владимировна - кандидат медицинских наук АО «Национальный научный кардиохирургический центр» заведующий отделением детской реабилитации.
3) Ибраев Талгат Ергалиевич - АО «Национальный научный кардиохирургический центр» заведующий отделением детской анестезиологии, реанимации и интенсивной терапии
4) Утегенов Галымжан Маликович - АО «Национальный научный кардиохирургический центр» кардиохирург
5) Мамежанова Людмила Ильинична - АО «Национальный научный кардиохирургический центр» кардиолог
6) Тулеутаева Райхан Есенжановна - кандидат медицинских наук РГП на ПХВ «Государственный медицинский университет города Семей», заведующая курсом клинической фармакологии, врач - клинический фармаколог.
Конфликт интересов: финансовая или другая заинтересованность в теме обсуждаемого документа отсутствует.
Рецензенты: Куатбеков Кайрат Ниеталиевич - кандидат медицинских наук, ГКП на ПХВ «Центр перинатологии и детской кардиохирургии» Управления здравоохранения города Алматы, заведующий отделением детской кардиохирургии, врач - кардиохирург высшей квалификационной кардиохирургии, главный специалист по детской кардиохирургии Управление здравоохранения города Алматы.
Условия пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1.
Внимание!
- Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
- Информация, размещенная на сайте MedElement, не может и не должна заменять очную консультацию врача. Обязательно обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
- Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может назначить нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
- Сайт MedElement является исключительно информационно-справочным ресурсом. Информация, размещенная на данном сайте, не должна использоваться для самовольного изменения предписаний врача.
- Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший в результате использования данного сайта.
Транспозиция магистральных сосудов (далее ТМС, ТМА) у новорожденных детей бывает двух видов. Первый — аномалия, при которой от анатомически правого желудочка начинается аорта, от анатомически левого — легочная артерия (далее ЛА). Порок характеризуется только аномальными пространственными отношениями магистральных сосудов. Предсердия, предсердно-желудочковые клапаны, желудочки сформированы и расположены правильно.
Второй, более редкий — когда одновременно с «перепутанными» артериями предсердия, желудочки и клапаны тоже не на своем месте. Это звучит хуже, но на самом деле куда более благоприятная картина, потому что при такой ТМА гемодинамика практически не нарушена.
Рассмотрим оба варианта и расскажем о диагностике, анатомии, опасности этих пороков, а также в какие сроки и как именно они лечатся.
Корригированная транспозиция магистральных сосудов (код по МКБ-10 — Q20.5) – это врожденный сердечный порок, который проявляется несогласованностью (дискордантностью) между предсердиями и желудочками, а также желудочками и присердечными артериями.
Несмотря на несогласованное сообщение между камерами, кровоток имеет физиологичный характер – в аорту поступает артериальная кровь, в легочной ствол — венозная. Правое предсердие соединяется с желудочком через клапан, который анатомически является митральным, а правый желудочек имеет структуру левого. От него кровь поступает в легкие через легочную артерию.
Из легких легочные вены соединяются с левым предсердием. Между ним и желудочком имеется клапан, повторяющий структуру трехстворчатого, а сам желудочек анатомически представлен правым, а не левым. От него в аорту поступает артериальная кровь.
Отличия от некорригированной формы:
- Изоляции кругов кровообращения друг от друга не происходит;
- Аорта и легочной ствол не пересекаются, а идут параллельно;
- Наблюдается одновременное пересечение желудочков;
- Характерно нарушение строения проводящих волокон и развитие у пациентов различных видов аритмий.
Частота встречаемости составляет 0,5% всех врожденных пороков.
Гемодинамика
Изолированный порок не приводит к нарушению гемодинамики , поскольку органы получают кислород в нужном количестве, а венозный отток не имеет препятствий. Сущность порока выражается не в обратном строении сердечных клапанов и желудочков, а в неправильном распределении внутрисердечной нагрузки.
Правый желудочек, который анатомически является левым, начинает работать с удвоенной силой. В то же время коронарные артерии не в состоянии обеспечивать адекватный кровоток (правая желудочковая артерия значительно меньше левой), что приводит к его постепенной ишемии и развитию стенокардии.
Характерно и параллельное развитие пролапса митрального клапана, который анатомически является трехстворчатым и не приспособленным выдерживать большое давление.
Опасно ли у новорожденных?
 Поскольку разобщения кругов кровообращения не происходит, заболевание в большинстве случаев диагностируют на поздних сроках (на первом, втором десятилетии жизни). Средний возраст выявления – 12,5 лет. У части пациентов порок остается не выявленным в течение всей жизни.
Поскольку разобщения кругов кровообращения не происходит, заболевание в большинстве случаев диагностируют на поздних сроках (на первом, втором десятилетии жизни). Средний возраст выявления – 12,5 лет. У части пациентов порок остается не выявленным в течение всей жизни.
Состояние больных ухудшается при развитии аритмии и ишемии сердца. Аритмии сопровождают заболевание в 60% случаев (пароксизмальная тахикардия, мерцательная аритмия, блокады) и часто являются первым поводом обращения к врачу. У другой группы больных вследствие того, что правый желудочек выполняет работу левого и испытывает большие перегрузки, возникают боли в сердце по типу стенокардии.
Сроки будут зависеть от наличия сопутствующих пороков и осложнений. Для больных, имеющих дополнительные пороки (дефекты перегородок), характерны яркая симптоматика и раннее выявление заболевания, лечение требуется в первые 28 дней жизни. У остальных пациентов ввиду удовлетворительного общего состояния и малого количества жалоб лечение проводится в плановом порядке.
Лечение отличается, поскольку корригированная форма имеет свои особенности и сопровождается аритмией и ишемическими болевыми приступами. Терапия корригированной формы дополняется лечением данных осложнений.
Что такое некорригорованная (полная) ТМА?
Полная транспозиция магистральных сосудов (код по МКБ-10 — Q20.3) – это критический ВПС синего типа, который характеризуется обратным соединением между желудочками и присердечными артериями.
При пороке происходит полное разграничение кругов кровообращения вследствие инверсного расположения крупных артериальных стволов. Правый желудочек соединен с аортой, левый — с легочной артерией. Венозная кровь, минуя легкие, поступает во внутренние органы из правого желудочка и возвращается обратно по полым венам. Легкие получают из левого желудочка артериальную кровь, которая возвращается в него, минуя органы и ткани. Венозная кровь не становится артериальной, в то время как артериальная постепенно перенасыщается кислородом.
Синонимы : некорригированная ТМС, цианотическая ТМС, транспозиция магистральных артерий, ТМА.
В зависимости от сочетания с другими аномалиями выделяют ТМС, имеющую:
- интактную перегородку между желудочками;
- (далее ДМЖП);
- сочетание и ДМЖП.
Частота встречаемости порока: 5-7% от всех врожденных пороков сердца. У мальчиков бывает в 3 раза чаще, чем у девочек. Данный ВПС впервые описан в 1797 году M. Baillie, а определение впервые дал Abbott.
Анатомия
Аорта расположена спереди и чаще всего справа от легочной артерии и начинается от правого желудочка. ЛА находится позади аорты, начинаясь от левого желудочка. Оба магистральных сосуда идут параллельно друг другу (в норме они перекрещиваются).

Часто бывает аномальное отхождение коронарных сосудов . Полые вены подходят к правому предсердию, легочные вены – к левому (как в норме).
Гемодинамика
Круги кровообращения разобщены:
- Из правого желудочка в аорту течет венозная кровь . Она циркулирует по большому кругу кровообращения и приходит по полым венам к правому предсердию, откуда снова попадает в правый желудочек.
- Из левого желудочка в ЛА приходит артериальная кровь . Она циркулирует по малому кругу и по легочным венам через левое предсердие вновь поступает в левый желудочек. То есть в легких постоянно циркулирует оксигенированная кровь.
Смешивание крови 2 кругов циркуляции и, как следствие, совместимость с жизнью при такой гемодинамике возможны только при наличии сообщений на уровне каких-либо отделов сердца либо экстракардиально (вне сердца).
Это объясняет, почему возможна выживаемость плода во внутриутробном периоде . В этот период имеются временные особенности строения: овальное окно между предсердиями, артериальный проток между ЛА и аортой, а газообмен осуществляется в плаценте. Поэтому существование порока не сильно влияет на развитие плода.
После рождения ребенок лишается плаценты, фетальные (имеющиеся только у плода) сообщения закрываются. И далее возможно несколько вариантов развития патологии:

Перемещение крови на уровне какой-либо коммуникации всегда идет в 2 направлениях, иначе один из кругов полностью опустел бы.
Полезное видео о гемодинамике при транспозиции магистральных артерий:
Насколько это опасно?
Данный порок является критическим и несовместимым с жизнью. После рождения у ребенка развивается глубокая гипоксия, сопровождаемая переполнением малого круга. Большинство новорожденных погибают на первом или втором месяце.
Продолжительность жизни несколько увеличивается, если порок сопровождается наличием отверстия в сердечных перегородках – это позволяет кругам кровообращения сообщаться между собой. Такой дефект является необходимым для продолжения жизни в период подготовки к операции, но при отсутствии лечения порок быстро приводит к сердечной недостаточности.
Естественное течение
ТМС любой разновидности – критическое состояние, требующее вмешательства в раннем детском возрасте . В отсутствие хирургической операции 30% детей умирают в течение первой недели, 50% — в первый месяц, 70% — в течение полугода, 90% — до возраста в 1 год. Выживаемость определяется разновидностью порока.
Причины смерти: сердечная недостаточность, гипоксия, ацидоз, сопутствующая патология (ОРВИ, пневмония, сепсис).
В какие сроки требуется лечение?
Сроки лечения будут зависеть от того, имеется ли у ребенка отверстие между камерами сердца. Если дефект перегородки присутствует, операцию выполняют в первые 28 дней после рождения. Если дефекта нет, операцию планируют в первую неделю жизни. В некоторых случаях (при наличии узкопрофильного стационара и хирурга узкой специализации) операция может быть проведена плоду.
Причины и факторы риска
Точная причина не установлена. Предполагается генетическая наследственность, но отвечающий за это ген пока не обнаружен. Иногда причиной выступает спонтанная мутация, когда беременная не подвергалась никаким внешним воздействиям вроде рентгеновского излучения, инфекционных болезней, приема лекарств.
Факторы риска:
- беременные женщины после 40 лет;
- злоупотребление алкоголем во время беременности;
- инфекции в течение беременности;
- сахарный диабет;
- наследственная отягощенность.
Основная часть пациентов – мальчики, имеющие крупную при рождении массу. Чаще ТМА встречается у детей с хромосомными аномалиями и синдромом Дауна. Реже встречаются такие сопутствующие дефекты, как , сообщение между правым предсердием и левым желудочком.
Симптомы у детей и взрослых
Внешние признаки:

- Цианоз кожи, слизистых оболочек, который появляется сразу или в скором времени после рождения.
Этот признак отмечается у 100% больных, поэтому порок называют еще «синим».
Выраженность цианоза зависит от размера шунтового отверстия. Когда ребенок кричит, цианоз приобретает фиолетовый оттенок.
- Одышка у 100% больных.
- Нормальная или увеличенная масса тела при рождении. Однако к возрасту 1-3 месяца развивается гипотрофия из-за трудностей в кормлении таких детей, которые обусловлены гипоксемией и сердечной недостаточностью.
- Задержка моторного развития.
- Нередко отставание в умственном развитии.
- Повторные ОРВИ, пневмонии.
Признаки, выявляемые при физикальном обследовании:
- хрипы в легких;
- II тон громкий, нерасщепленный;
- при отсутствии сопутствующих пороков не слышны шумы в области сердца;
- при присутствии ДМЖП слышен систолический шум средней силы вдоль нижней половины левого края грудины, обусловленный сбросом крови сквозь ДМЖП;
- при наличии стеноза ЛА имеется систолический шум выброса (на основании сердца, тихий);
- тахикардия;
- увеличение размеров печени.
Диагностика
Лабораторные данные: при исследовании газов крови — тяжелая артериальная гипоксемия. Данные инструментальных методов представлены ниже.

Дифференциальная диагностика проводится с другими ВПС синего типа.
Как выявляют у плода: УЗИ и ЭКГ
| Метод | Время определения | Результаты |
| Определение толщины воротникового пространства | 12-14 неделя (1 триместр) | Толщина более 3.5 мм |
| Первый ультразвуковой скрининг | 1 триместр | Нарушение эмбриональной закладки сердца и крупных сосудов |
| Второй ультразвуковой скрининг | 2 триместр | Сформированная транспозиция сосудов, задержка роста плода |
| Цветовое допплеровское картирование | 2 триместр | Разобщение кругов кровообращения, транспозиция сосудов |
| УЗИ сердца (фетальная эхокардиография) | 2 триместр | Разобщение кругов кровообращения, транспозиция сосудов, «яйцеобразное» сердце |
| Непрямая электрокардиография | 2 триместр | Смещение электрической оси сердца влево, признаки блокады сердца |
В случае подтверждения диагноза проводится врачебный консилиум. Дальнейшая тактика:
- Беременная получает исчерпывающую информацию о пороке, перспективах лечения и возможных рисках операции;
- К моменту родов женщина госпитализируется в роддом, имеющий отделения реанимации и сердечно-сосудистой хирургии;
- После родоразрешения выполняется оперативное вмешательство.
Лечение
Заболевание всегда проявляется в период новорожденности. Скорость ухудшения состояния ребенка зависит от наличия и размеров сопутствующих дефектов, обусловливающих сообщение между двумя кругами циркуляции. Лечение только хирургическое . При установлении диагноза показания абсолютные.
Предоперационная подготовка
- Получение данных о насыщении артериальной крови кислородом и ее рН.
- Мероприятия по коррекции метаболического ацидоза, гипогликемии.
- Внутривенная инфузия препаратов простагландина Е1. Это препятствует закрытию артериального протока, и сохраняется возможность смешения крови. Мера является лишь кратковременной альтернативой процедуре Рашкинда.
- При тяжелой гипоксии – оксигенотерапия.
- Оценка состояния почек, печени, кишечника и мозга.
Методы хирургического вмешательства можно разделить на корригирующие и паллиативные .
Паллиативные операции
Паллиативные операции призваны:
- уменьшать гипоксемию путем улучшения обмена кровью между правыми и левыми отделами сердца;
- создавать хорошие условия для работы малого круга кровообращения;
- быть технически простыми и не создавать в будущем препятствий для проведения корригирующей операции.
Таким требованиям удовлетворяют различные методы расширения или создания ДМПП. Из них наиболее распространены операция Рашкинда и метод по Парку .
В случаях, когда у ребенка есть ДМПП достаточного размера, коррекция порока может быть произведена без паллиативных вмешательств. В остальных случаях корригирующей операции обычно предшествуют паллиативные вмешательства.
Операция Рашкинда
У больных без ДМПП и ДМЖП операцию нужно выполнить сразу после их поступления в кардиохирургический центр. Повышение оксигенации крови, полученное с помощью этой процедуры, дает свободу выбора срока корригирующей операции в пределах 7-20 дней после рождения.
 Ход операции:
Ход операции:
- Через бедренную и нижнюю полую вену внутрь правого предсердия вводится сложенный баллон.
- Через овальное отверстие его проталкивают в левое предсердие, где он заполняется жидким рентгеноконтрастным веществом и резко возвращается в расправленном виде в правый отдел под рентген- или эхоскопическим контролем. При этом происходит отрыв заслонки овального отверстия.
Преимущество процедуры в том, что отсутствует рассечение грудной клетки, которое обычно обусловливает развитие спаек в этой области, а это утяжеляет в последующем проведение корригирующей операции (затрудняется торакотомия, выделение сердца).
Техника по Парку
При возрасте ребенка более 30 дней должный эффект от операции Рашкинда часто не достигается в связи с тем, что заслонка овального окна плотно фиксирована к перегородке, а также в связи с большей прочностью межпредсердной перегородки. В этих случаях применяется техника по Парку.
С помощью встроенного на конце катетера лезвия разрезают перегородку между предсердиями, а затем выполняют расширение с помощью баллона.
Полная коррекция артерий
Корригирующие операции должны кардинально исправить нарушенную гемодинамику и устранить компенсирующие и сопутствующие пороки. К основным таким вмешательствам относятся артериальное переключение и внутрипредсердная коррекция.
Артериальное переключение
Суть: истинная анатомическая коррекция ТМС. Оптимальное время проведения: первый месяц жизни.
 Ход операции:
Ход операции:
- После введения пациента в наркоз и рассечения грудной клетки, начинают искусственное кровообращение, которым параллельно охлаждают кровь.
- При уменьшении температуры замедляется обмен веществ, и это защищает организм от послеоперационных осложнений. Разрезаются аорта и ЛА.
- От аорты отделяют коронарные сосуды и соединяют с началом ЛА, которое потом станет началом новой аорты. Сюда подшивают отрезанную аорту. Затем из кусочка перикарда пациента создают трубку, вшиваемую в новую ЛА и восстанавливающую ее.
Основные осложнения: надклапанный стеноз аорты, ЛА; недостаточность аортального клапана и/или клапана ЛА; нарушения сердечного ритма.
Методы внутрипредсердной коррекции (Мастарда и Сеннинга)
Они длительное время являлись единственными способами хирургического лечения транспозиции магистральных артерий. Сейчас эти операции применяются, когда нет возможности произвести полное анатомическое исправление порока .
Суть: исправление гемодинамики, сам порок анатомически не исправляется.
Ход операции : рассекают правое предсердие, удаляют полностью межпредсердную перегородку и вшивают внутри образовавшейся полости заплатки из тканей пациента (часть стенки предсердия, перикарда). В результате кровь через полые вены идет в левый желудочек, легочную артерию и легкие, из легочных вен — в правый желудочек, аорту и большой круг.
Дополнительные корригирующие операции: пластика ДМЖП, коррекция стеноза ЛА.
Полезное видео о коррекции ТМА:
Прогнозы и летальность после операции, длительность и качество жизни
Прогноз после оперативного вмешательства при обоих пороках относительно благоприятный. У пациентов с полной транспозицией наблюдаются замедление физического развития, отставание в росте, снижение иммунитета, склонность к инфекционным заболеваниям несмотря на проведенную терапию.
Продолжительность жизни в зависимости от полноценности операции может быть не сокращена, но чаще наблюдается уменьшение ее на 10-15 лет. Пациенты, доживающие до зрелого и пожилого возраста, пожизненно придерживаются индивидуальных врачебных рекомендаций.
У людей с корригированной формой срок жизни не изменен. Пациенты из данной группы доживают до зрелого и пожилого возраста (70 и более лет). Качество жизни изменяется незначительно – оперированные находятся на учете у кардиолога, проходят курсы лечения по поводу аритмии, стенокардии и других сопутствующих заболеваний.
Летальность при операциях:
- Операция Рашкинда – 9%;
- Операция Парка – 13%;
- Операция Мастарда – 25%;
- Артериальное переключение — 10%.
Ближайшие и отдаленные последствия коррекции
Ближайшие последствия:
- Повреждения коронарных артерий;
- Разрывы волокон миокарда и мелкоочаговые инфаркты;
- Аритмия.
Отдаленные последствия:

- Полная атриовентрикулярная блокада;
- Острая и хроническая сердечная недостаточность;
- Предсердная пароксизмальная тахикардия;
- Трепетание и фибрилляция желудочков;
- Задержка в развитии;
- Пролабирование митральных створок.
Наиболее частыми причинами отрицательных последствий являются:
- Травматические повреждения венечных сосудов;
- Неполное устранение сопутствующей патологии — дефекта перегородок, митральной недостаточности;
- Разрыв проводящих нервных волокон (пучков Гиса, волокон Пуркинье).
Наблюдение
Прооперированные пациенты наблюдаются пожизненно . Интервал — 6-12 месяцев. Цель — своевременное обнаружение осложнений. В первые полгода после операции или при появлении осложнений в отдаленном периоде проводится профилактика бактериального эндокардита.
Транспозиция магистральных сосудов характеризуется быстрым развитием тяжелых осложнений, критично нарушающих работу сердечно-сосудистой системы. Без лечения дети погибают в раннем возрасте. Поэтому необходимо принятие неотложных консервативных и хирургических мер по коррекции ТМС с учетом его типа.
— патология сердца, которая носит врожденный характер и заключается в том, что две основные артерии, которые исходят из сердца, поменялись местами. Меняется кровоток в организме, в результате организм ощущает недостаток поступления кислорода к тканям.
Выявляют в течение первых дней жизни ребенка. После выявления транспозиции магистральных сосудов необходимо делать операцию на сердце ребенка для устранения данной патологии, обычно операцию делают на первый день жизни ребенка.
Транспозиция магистральных сосудов проявляет себя через синюшность кожных покровов, одышку, отсутствие аппетита, плохой прибавкой в весе.
Если признаки и симптомы транспозиции магистральных сосудов не появились в роддоме, то при появлении хотя бы одного признака следует обратиться к врачу .
Причины транспозиции магистральных сосудов
 является пороком сердца, если здоровы родители, в их ДНК нет генетических мутаций, то говорят о единичном случае мутации генов, причина в большинстве случаев неизвестна. Этот порок возникает еще в утробе матери на этапе формирования сердца и сосудов, то есть в первые 45 дней беременности.
является пороком сердца, если здоровы родители, в их ДНК нет генетических мутаций, то говорят о единичном случае мутации генов, причина в большинстве случаев неизвестна. Этот порок возникает еще в утробе матери на этапе формирования сердца и сосудов, то есть в первые 45 дней беременности.
Легочная артерия, которая несет кровь не богатую кислородом, исходит из правого желудочка. Затем кровь, которая обогатилась кислородом, продолжает свой путь по легочной вене в левое предсердие. Далее кровь попадает в левый желудочек, из которого выходит аорта, являющаяся самой крупной артерией у человека. Из аорты выходят остальные артерии, по которым кровь бежит ко всем системам органов и органам, тканям и клеткам.
Нарушает нормальное месторасположение сосудов: легочная артерия отходит от левого желудочка, аорта от правого. Кровь не обогащенная кислородом идет по аорте из правых отделов сердца, не проходя к легким, а кровь, идущая по легочной артерии из левого желудочка, которая обогащена кислородом, попадает вновь в легкие и обратно в левое предсердие и желудочек.
Когда по большому кругу кровообращения циркулирует бедная кислородом кровь, кожные покровы приобретают синюшный цвет, такое состояние получило название — циноз.
Факторы риска возникновения транспозиции магистральных сосудов
Точная причина неизвестна, хотя некоторые факторы могут увеличить риск развития такой патологии у ребенка:
- краснуха, грипп во время беременности
- генетическая предрасположенность
- недостаточное потребление белков и витаминов во время беременности
- употребление алкоголя во время беременности
- возраст матери старше 40 лет
- наличие сахарного диабета
- синдром Дауна у новорожденного
Осложнения транспозиции магистральных сосудов.
Существует множество осложнений транспозиции магистральных сосудов : кислородное голодание тканей, сердечная недостаточность, поражение легких (затрудненность дыхания). В тяжелых случаях может привести к летальному исходу, если не осуществить своевременную операцию. У перенесших операцию в дальнейшем могут появиться пороки клапанов сердца, сужение коронарных артерий, различные нарушения ритма сердца, развиться сердечная недостаточность.
Диагностика транспозиции магистральных сосудов

При рождении ребенка врач может практически сразу выявить такой дефект по синюшности кожи, нарушению дыхания. Однако синюшности кожи может и не быть, если у ребенка развивается другой порок сердца, например, большой дефект межпредсердной перегородки, в результате определенная часть крови, которая обогащена кислородом, попадает в большой круг кровообращения.
Ребенок растет и не позволяет ему развиваться, расти, так как не дает кровеносной системе обеспечить адекватный кровоток обогащенной кислородом крови. Для диагностики и выявления пороков сердца также используется аускультация. Физикального обследования недостаточно для постановки правильного диагноза — транспозиции магистральных сосудов. Проводится обследование с помощью других методов:
- эхокардиографии — исследование сердца с помощью узи, это безопасный и недорогой вариант обследования, при этом дает много необходимой информации врачу, благодаря эхокардиографии возможно определить откуда исходят аорта и легочная артерия. При этом эхокардиография помогает выявить другие пороки сердца;
- рентгенография грудной клетки, которая позволяет оценить размеры сердца новорожденного и положение легочной артерии;
- экг, необходим для выявления различных патологий сердца, производят регистрацию электрических потенциалов сердца, что дает информацию о работе сердца, состояния желудочков, а также позволяет выявить нарушения ритма сердца;
- коронарография представляет рентгенографический метод, который заключается в том, что с помощью катетера в кровоток вводится специальное рентгеноконтрастное вещество, делается серия ренгеновских снимков.
Лечение транспозиции магистральных артерий
Транспозиция магистральных артерий
лечится только хирургическим путем.
До операции проводится терапия, которая направлена на облегчение состояния ребенка перед операцией. Вводят препарат простагландина Е1(Аппростадил), который помогает протоку между аортой и легочной артерией оставаться не заращенными, что позволяет обеспечить нормальный кровоток у новорожденного до операции.
Также делают артериальную септостомию. Она заключается в том, что при катетеризации сердца производят расширение естественного отверстия в межпредсердной перегородке. Это позволяет обеспечить кровоток между большим и малым кругом кровообращения.
Хирургическое лечение транспозиции магистральных артерий
Операция при лечении транспозиции магистральных сосудов включает в себя операции артериального переключения, операции на предсердиях. Операция артериального переключения производят в первые месяцы жизни новорожденного. Хирург перемещает аорту и легочную артерию на свои места. Легочная артерия подсоединяется к правому желудочку, а аорта к левому. Коронарные артерии подшиваются к аорте. Операция на предсердиях — хирург создает туннель между двумя предсердиями, это помогает направить кровь не насыщенную кислородом в левый желудочек и легочную артерию для того, чтобы она насытилась кровью в легких. Правый желудочек должен качать кровь по всему телу, а не только в легкие, как в норме. Возможным осложнением операции на предсердиях во время транспозиции магистральных сосудов является нарушение ритма сердца и проблемы с правым желудочком.
После операции транспозиции магистральных артерий
После операции ребенок должен наблюдаться у врача-кардиолога, ему необходимо избегать чрезмерных физических нагрузок. Кроме того, тем, кто перенес операции по коррекции транспозиции магистральных артерий, необходимо применять антибиотики при любых других хирургических и стоматологических операциях, это обеспечит профилактику инфекционных осложнений со стороны сердца. Пациентам, которые перенесли операцию на предсердиях, не требуется такая профилактика.
Или сокращённо ТМС – это один из видов врождённых пороков развития сердца , при котором магистральные сосуды (аорта и ) отходят от сердца в неправильном порядке. Данный порок развития может быть обнаружен уже на самых ранних этапах развития беременности, поэтому довольно часто молодые мамочки узнают об этой проблеме задолго до родов. В этой статье мы постараемся объяснить, что такое транспозиция магистральных сосудов, может ли ребёнок родиться и жить с таким диагнозом, и что нужно делать а этом случае?
Транспозиция магистральных сосудов бывает нескольких типов: простая, ТМС в сочетании с дефектами перегородок сердца и корригированная ТМС. К критическим порокам, требующим лечения в первые дни жизни относится простая ТМС.
При ТМС сосуды полностью меняются своими местами, то есть аорта отходит от правого желудочка сердца, а – от левого желудочка. В этом случае оба круга кровообращения (большой и легочный) оказываются совершенно изолированными друг от друга. Получается что кровь легочного круга всё время обогащается кислородом, но в большой круг не попадает. А кровь из большого круга кровообращения, бедная кислородом, не может попасть в лёгкие. В такой ситуации жизнь ребенка была бы невозможна.
Авторские права на представленный материал принадлежат сайтуВсе-таки при ТМС кровь между кругами кровообращения может смешиваться. В частности кровь в малый (легочный) круг кровообращения может попадать через . Этот сосуд функционирует у всех детей во время внутриутробного развития, а после рождения закрывается. Существуют препараты, способные поддерживать артериальный проток открытым. Поэтому очень важно, чтобы ребенок с простой ТМС получал эти лекарства. Это позволит стабилизировать состояние ребенка до операции.
До рождения ребёнка, на этапе внутриутробного развития , такой ВПС не мешает жить и развиваться плоду, поскольку у плода легочный круг кровообращения практически не функционирует, вся кровь циркулирует только по большому кругу через и открытый артериальный проток . Поэтому дети рождаются доношенными, совершенно нормальными, но сразу очень синюшными.
После рождения и первого вздоха ситуация резко меняется – начинает функционировать отдельно легочной круг кровообращения, а размера становится недостаточно чтобы смешивать кровь в большом и малом круге. К тому же, с каждым часом становится всё меньше, что усугубляет ситуацию. Поэтому дети с простой транспозицией магистральных сосудов находятся в опасном для жизни положении и им требуется срочная сразу после родов .
Конечно, если ТМС сочетается с другими пороками развития сердца, например или ДМЖП, то эта ситуация более выгодна для новорожденного, так как эти дефекты позволяют потоку крови перетекать из одного круга в другой, поэтому у них угроза для жизни становится не такой сильной, и у хирургов есть время чтобы выбрать правильную тактику оперативного лечения . Однако в любом случае, при полной транспозиции магистральных сосудов операция необходима , вопрос только в том, когда её делать – сразу после родов, или можно подождать.
Поэтому если во время беременности Вы узнали, что у плода может быть транспозиция магистральных сосудов , то самое главное, что необходимо сделать – найти специализированный роддом, который сотрудничает с кардиоцентром с тем, чтобы ребёнку можно было провести операцию на сразу после . Подобные родильные дома есть в основных крупных городах, таких как Москва, Санкт-Петербург, Новосибирск, Томск, Пенза, Самара.
Однако важно понимать, что радикальная коррекция полной ТМС – довольно сложная операция, которая успешно выполняется лишь в некоторых городах нашей страны. Во всех остальных кардиоцентрах могут выполнить лишь процедуру Рашкинда – это вспомогательная операция, которая устраняет критическую ситуацию и даёт возможно ребёнку с ТМС прожить ещё несколько недель. Однако для полной коррекции ТМС, ребёнка всё равно необходимо транспортировать в один из городов, где расположены ведущие нашей страны. Мы можем порекомендовать Москву, Новосибирск, Томск, Самару, Пензу.
Помните, что сложнейшая операция для полной коррекции ТМС, должна быть выполнена в течении первого месяца жизни ! Позже становится проблематичным выполнить радикальную коррекцию, т.к. левый желудочек «отвыкает» работать, как системный и после радикальной операции может не справится с нагрузкой. Поэтому, если сроки радикальной коррекции упущены, ребенку сначала выполняется вспомогательная операция, которая подготавливает левый желудочек к радикальной коррекции.
Другим подвидом транспозиции магистральных сосудов является корригированная ТМС . В этом случае природа как бы ошиблась дважды: перепутаны оказались не аорта с легочной артерией, а желудочки сердца. При корригированной ТМС венозная кровь приходит в левый желудочек, но от него отходит легочная артерия, а артериальная кровь из легких возвращается в правый желудочек, но от него отходит аорта. То есть кровообращение не страдает. Ребенок выглядит абсолютно здоровым. Проблемы возникают позже. Дело в том, что правый желудочек не приспособлен работать на большой круг кровообращения. Со временем функция правого желудочка ухудшается
Так как оба круга кровообращения функционируют нормально, то опасной для жизни ситуации в этом случае не возникает и дети могут жить без операции очень долго. У нас на форуме родителей детей с ВПС есть участники, которым уже более 30 лет и у них коррегированная ТМС . Однако некоторые проблемы у таких детей могут быть. Например, то что правый желудочек сердца анатомически не предназначен для кровоснабжения большого круга, приводит к тому что эти дети всё же отстают в развитии по сравнению со здоровыми детьми хотя и незначительно. Также корригированная ТМС часто сочетается с другими аномалиями сердца (дефектами межжелудочковой перегородки и т.п.)




